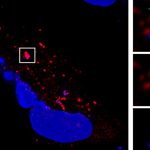
La mayoría de las muertes que provocó la gripe española de 1918 y la pandemia de gripe A (H1N1) de 2009–2010 se asoció a una infección bacteriana secundaria por neumococo. Ahora, un estudio internacional liderado por científicos de Córdoba arroja luz a mecanismos moleculares que regulan este proceso y abre caminos para mejorar el tratamiento de pacientes que padezcan esa coinfección.
(Agencia CyTA-Leloir)-. Un estudio internacional liderado por científicos argentinos abre caminos para mejorar en el futuro el tratamiento de pacientes con gripe por virus influenza A que presentan infecciones secundarias bacterianas causadas por el neumococo (Streptococcus pneumoniae).
La mayoría de los 40 a 50 millones de muertes provocadas durante la pandemia de influenza A en 1918, conocida como la conocida como “la gripe española”, se asoció a una infección bacteriana secundaria por neumococo. Lo mismo se evidenció con las muertes de la pandemia de gripe A (H1N1) de 2009–2010 causada por una variante del virus (subtipo H1N1). Se sabe que hay una sinergia entre ambos patógenos, pero se conoce poco sobre los mecanismos que regulan esa “convivencia”.
Investigadores del Centro de Investigación en Bioquímica Clínica e Inmunología (CIBICI) no solo identificaron cómo el virus influenza A prepara el terreno para que el neumococo pueda proliferar en las células, sino que ahora también descubrieron estrategias que la bacteria misma despliega para prevalecer en un medio celular hostil.
“A la luz de nuestros resultados, proponemos que los antibióticos intracelulares también deben ser considerados para el tratamiento de infecciones neumocócicas durante una epidemia o una pandemia de influenza A”, afirma José Echenique, director del trabajo y jefe de laboratorio en el CIBICI, que depende del CONICET, y en el Departamento de Bioquímica Clínica de la Facultad de Ciencias Químicas de la Universidad Nacional de Córdoba (UNC).
Una sinergia peligrosa
En un trabajo previo y realizando experimentos con cultivos de células, Echenique y colegas comprobaron que el virus de influenza A bloquea la capacidad la autofagia, un mecanismo que la célula usa para atrapar a los neumococos y destruirlos.
Ahora, tal como revela la revista PLOS Pathogens, Echenique y colegas lograron describir un sistema de percepción de señales del neumococo, denominado SirRH, que regula la expresión de más de 100 genes del neumococo. Y vieron que dos de ellos, ClpL y PsaB, despliegan respuestas de adaptación al estrés ácido y oxidativo del medio intracelular en células infectadas con virus influenza A para sobrevivir y replicarse. “La actividad de esos genes del neumococo favorece la relación sinérgica con el virus influenza A”, indicó Echenique.
El estudio cobra relevancia si se considera que la gripe estacional producida por el virus influenza infecta por año cerca de mil millones de personas y ocasiona de 3 a 5 millones de infecciones graves, con 500 mil muertes. Y si bien hay una vacuna y una variedad de antibióticos contra el neumococo, esta bacteria, que habita normalmente en la nasofaringe humana y produce infecciones leves como sinusitis y otitis, también causa infecciones graves como neumonía y meningitis y mata 1,5 millones de personas por año.
“Estos hallazgos tienen implicaciones importantes para comprender las infecciones secundarias bacterianas en pacientes con influenza y pueden inspirar el desarrollo de nuevas aplicaciones terapéuticas”, afirmó Echenique.
El primer autor del estudio es Nicolás Reinoso-Vizcaíno, integrante del CIBICI, Y también participaron Paulo Cortes, Nadia Olivero y Mirelys Hernández-Morfa, del CIBICI; Melina Cian, del CIBICI y de la Universidad de Oklahoma, en Estados Unidos; Germán Piñas., del CIBICI y de la Universidad de Utah; Daniel Perez, científico cordobés en la Universidad de Georgia, Estados Unidos; Chandan Badapanda y Ankita Rathore, de Xcelris Labs Limited, en India.