Así lo afirma la bioquímica y doctora en Medicina Roxana Gabriela Vitale, Investigadora del CONICET, responsable del Sector de Micología de la Unidad de Parasitología del Hospital JM Ramos Mejía, en la Ciudad de Buenos Aires, y una de las autoras de la última versión del Atlas de Micología Clínica que describe más de 700 especies de hongos que causan enfermedades fúngicas.
(Agencia CyTA-Leloir. Por Bruno Geller)-. En la India, más de 9000 pacientes fueron diagnosticados con una infección fúngica que popularmente se conoce con el nombre de “hongo negro”, la mayoría de los cuales padecían diabetes no controlada. Y luego se detectaron casos aislados en países como Uruguay, Estados Unidos, Brasil, México, España, Italia, Austria, Irán y, más recientemente, Argentina.
“La enfermedad es conocida técnicamente como mucormicosis y es de distribución mundial. El ‘hongo negro’ pertenece al orden de los hongos hialinos ‘Mucorales’ en el que se agrupan distintos géneros y especies como Mucor, Rhizopus, Lichteimia o Cunninghamella, entre otros. El hongo penetra en los vasos sanguíneos y puede ocasionar necrosis o muerte de tejido, afectando los senos paranasales, la región orbital y hasta al cerebro”, explicó la bioquímica y doctora en Medicina Roxana Gabriela Vitale, investigadora del CONICET, responsable del Sector de Micología de la Unidad de Parasitología del Hospital JM Ramos Mejía, en la Ciudad de Buenos Aires.
“Es importante que se tome conocimiento sobre la coinfección fúngica en pacientes con COVID-19 y se focalice si existe o no una comorbilidad previa. Se debe estar atento ante la aparición de cualquier síntoma, aun cuando el paciente haya sido dado de alta después de haber estado internado por largo tiempo y haber recibido terapia con corticoides”, enfatizó Vitale, una de las autoras de la última versión del Atlas de Micología Clínica que describe más de 700 especies de hongos que causan enfermedades fúngicas.
De esta manera, afirmó la especialista, se podrá sospechar y hacer un diagnóstico más rápido que permita un tratamiento antifúngico adecuado basado en la evaluación clínica, exámenes histológicos y cultivo. “No puede sospecharse lo que se no se conoce”, agregó.
La mucormicosis no es una nueva patología, y no sólo se relaciona con pacientes diabéticos que entran en cetoacidosis (altos niveles de acidez en sangre), sino también en aquellos que presenten algún tipo de inmunosupresión como por ejemplo, pacientes con cáncer bajo tratamiento con quimioterapia, con enfermedades autoinmunes o que sufrieron quemaduras graves.
“El diagnóstico precoz es clave”
En pacientes críticamente enfermos con neumonía viral grave, las coinfecciones son complicaciones bien conocidas, puntualizó Vitale.
Vitale también se refirió a la aspergilosis pulmonar invasiva asociada a COVID-19, coinfección que se denomina con las siglas CAPA (por sus siglas en inglés) “y que requiere un pronto diagnóstico para administrar un tratamiento de manera oportuna”.
También se han reportado casos de pacientes con COVID-19 con presencia de hongos en sangre (fungemia) ocasionada por levaduras del género Candida spp., y levaduras no Candida como por ejemplo, Trichosporon spp., Cryptococcus, Rhodotorula spp y Sacharomyces. Otras infecciones en pacientes con COVID-19 reportadas fueron micosis sistémicas endémicas y neumocistosis (infección pulmonar provocada por el hongo Pneumocystis jirovecii).
Vitale agregó que hay varios factores predisponentes que facilitan la coinfección con hongos: largos períodos de internación en terapia intensiva, administración de corticoides y antibióticos de amplio espectro, epitelio respiratorio dañado, disfunción mucociliar, daño alveolar, desregulación inmunológica, parálisis inmunitaria local y comorbilidades, entre otros. “Por este motivo es de sospechar y esperar la asociación de COVID-19 con estas infecciones”, manifestó la especialista.
Los hongos se encuentran distribuidos por todo el mundo, en el ambiente, en suelo, en plantas o alimentos en descomposición. “Convivimos con estos hongos a diario, no son nuevos ni han aparecido por el coronavirus. Tampoco se contagian entre personas. La asociación infección fúngica-COVID-19 se evidencia más en aquellos pacientes que tuvieron una larga internación en terapia intensiva y recibieron una terapia prolongada de esteroides”, concluyó Vitale, doctorada en el Centro Médico de la Universidad Radboud de Nimegen y en el Instituto de Biodiversidad Fúngica Westerdijk (antes Centro de Biodiversidad Fúngica, CBS), en Utrecht, Países Bajos.

Roxana Gabriela Vitale, bioquímica, doctora en medicina, investigadora del CONICET y responsable del Sector de Micología de la Unidad de Parasitología del Hospital JM Ramos Mejía, en la ciudad de Buenos Aires.
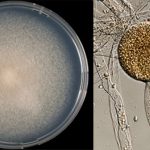
Colonias e imagen de microscopia de Mucor, el llamado “hongo negro”. Créditos: Imágenes presentadas con permiso de los autores del Atlas of Clinical Fungi. 2020. de Hoog GS, Guarro J, Gené J, Ahmed S, Al-Hatmi AMS, Figueras MJ, Vitale RG. Atlas of Clinical Fungi, 4th e-edition. Foundation Atlas of Clinical Fungi, Hilversum, The Netherlands.


